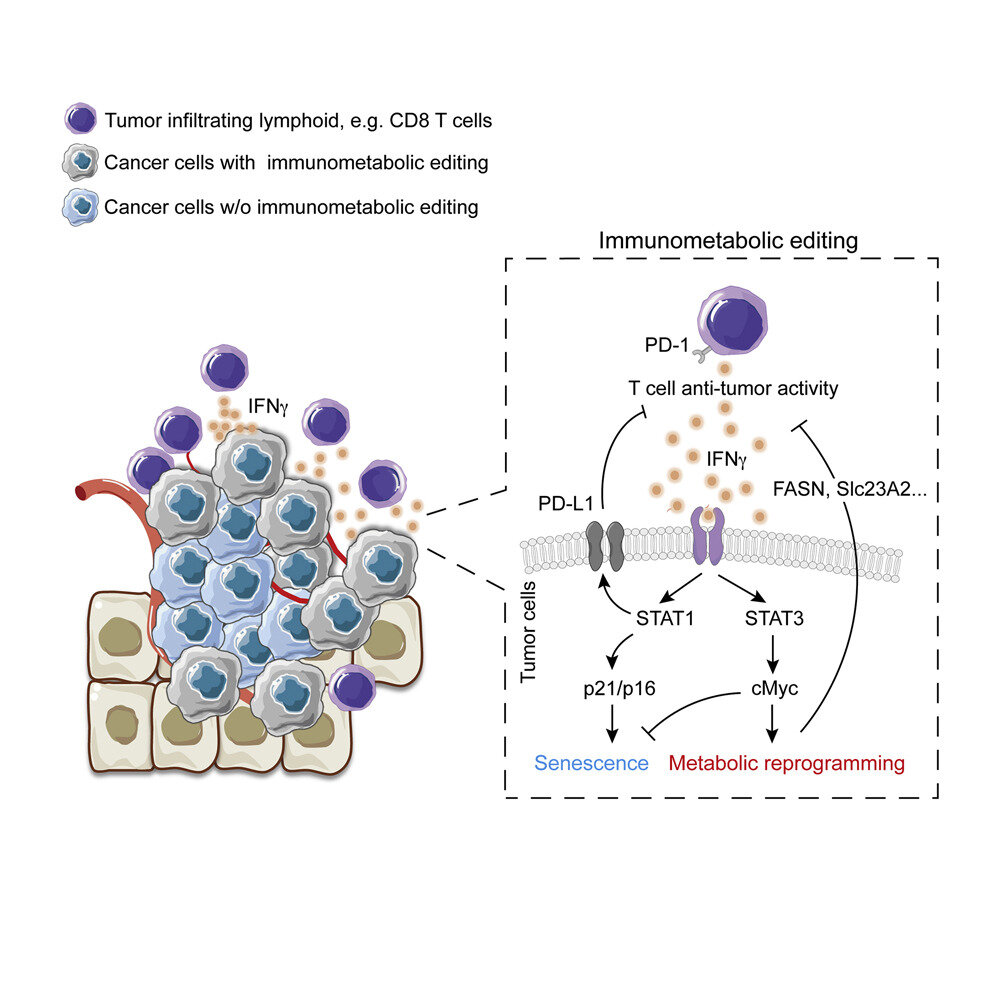
В ходе исследования, проведенного в рамках программы Ludwig Cancer Research, было обнаружено, что иммунная система, следящая за раком, может сама вызывать метаболические изменения в клетках опухолей на ранних стадиях, которые одновременно способствуют их росту и позволяют им подавлять смертельные иммунные реакции. В исследовании, опубликованном в журнале Cell Metabolism под руководством члена-корреспондента Лозаннского университета Людвига Пинг-Чих Хо, подробно описывается точный механизм, с помощью которого происходит "иммунометаболическое редактирование" зарождающихся опухолей в мышиных моделях рака кожи - меланомы, и определяется новый биохимический сигнальный каскад и белки, которые регулируют его действие. Помимо освещения ранее неизвестного аспекта эволюции опухолей, полученные результаты открывают большие перспективы для повышения эффективности иммунотерапии рака.
"Мы обнаружили десятки метаболических ферментов, которые способствуют уклонению от иммунитета в опухолях меланомы", - говорит Хо. "Эти ферменты, а также некоторые отдельные компоненты выявленного нами сигнального пути представляют собой богатый арсенал потенциальных лекарственных мишеней для подрыва защиты, воздвигнутой иммунометаболическим редактированием. Такие препараты могут сделать опухоли уязвимыми для иммунной очистки, а также могут быть использованы в сочетании с блокадой контрольных точек и другими иммунотерапиями для преодоления устойчивости большинства раковых опухолей к таким методам лечения". Считается, что наблюдение иммунной системы за раковыми опухолями способствует возникновению злокачественных опухолей, стимулируя эволюцию раковых клеток, которые могут подорвать механизм иммунного обнаружения и атаки. Эта теория "иммуноредактирования", разработанная, в частности, бывшим научным директором и генеральным директором Института Людвига по исследованию рака, покойным Ллойдом Олдом, и членом Научно-консультативного комитета Людвига Робертом Шрайбером, в настоящее время является фундаментальным принципом иммунологии опухолей. Исследователи также давно знают, что метаболические адаптации, характерные для раковых клеток - например, их активное потребление сахара глюкозы - подрывают противоопухолевые иммунные реакции. Однако оставалось неясным, может ли иммунный надзор также вызывать метаболические адаптации в раковых клетках и могут ли эти адаптации дополнительно помочь им противостоять иммунным реакциям. Именно это и было установлено в настоящем исследовании, раскрывающем ту грань эволюции опухолей, которая предполагалась, но до сих пор оставалась недоказанной. Хо и его коллеги выявили три ключевых белка, которые обеспечивают этот эффект: IFNγ, STAT3 и c-Myc. IFNγ, являющийся инструментом противоракового надзора, выделяется Т-клетками и другими иммунными клетками и, как известно, блокирует рост раковых клеток. Но сигналы, которые он вызывает, опосредованные белком STAT1, также вызывают адаптацию раковых клеток, которая помогает им уклоняться от атаки Т-клеток - процесс, известный как иммуноредактирование. В настоящем исследовании ученые показали, что IFNγ дополнительно активирует отдельный и малоизученный сигнальный путь, опосредованный родственным белком STAT3. Этот путь изменяет экспрессию генома раковой клетки, вызывая "эпигенетические" изменения, которые определяют, какие гены активны. Он также гиперактивирует главный регулятор клеточного метаболизма, известный как c-Myc, который сверхэкспрессируется во многих видах рака. Исследователи показали, что гены, активированные c-Myc, не только определяют метаболизм рака, но и нарушают проникновение Т-клеток в опухоли и препятствуют их атаке на раковые клетки. Сигнальные пути, опосредованные STAT1 и STAT3, фактически, синергично наделяют возникающие опухоли критической способностью избегать иммунного клиренса, стимулируя иммунометаболическое редактирование, которое способствует их эволюции в полноценную злокачественную опухоль. "Предыдущие исследования показали, что потеря активности STAT3 в раковых клетках способствует иммунной инфильтрации и вызывает регрессию опухоли", - сказал Хо. "Наши результаты объясняют причину этого и позволяют предположить, что воздействие на STAT3 с помощью лекарств может восстановить чувствительность к IFNγ в раковых клетках, которые развились за пределами его ингибирующей способности". Исследователи также использовали CRISPR редактирование генома для скрининга 2 078 метаболических ферментов в опухолях мышей и выявили 40 метаболических генов, контролируемых c-Myc, которые играют важную роль в помощи раковым клеткам уклоняться от иммунного контроля и атаки. Эти ферменты также являются основными кандидатами для нацеливания на лекарства. "Помимо фармакологических последствий, - говорит Хо, - это исследование раскрывает ранее недооцененный аспект иммуноредактирования, который повлияет на наше понимание метаболического взаимодействия между раковыми клетками и иммунными клетками в микроокружении опухоли". | |
| Просмотров: 270 | |